Moderna to apply today for FDA authorization for its COVID-19 vaccine
【聖路易時報訊】由Moderna藥廠開發之新冠病毒疫苗,今天(11月30日)正式向美國食品藥物管理局(FDA)提出申請緊急授權使用,FDA將於12月17日開會審查。 這是繼11月20日輝瑞藥廠(Pfizer)申請新冠病毒疫苗使用後,第二支疫苗申請緊急使用。輝瑞藥廠疫苗FDA審核會議將於12月10日開會審查。
據Moderna藥廠向FDA所提出的第三期臨床檢測試驗數據顯示,該藥廠疫苗對預防新冠病毒的有效性為94.1%,對預防嚴重病症有效率更達100%。

Moderna藥廠今天也向歐洲藥品管理局申請疫苗之使用授權。
預計在今年年底,Moderna藥廠可在美國將提供約2千萬劑疫苗,明年在全球製造5億至10億劑疫苗。
美國國家過敏和傳染病研究所(National Institute of Allergy and Infectious Diseases)所長、美國防疫最高專家Anthony Fauci醫師表示,預計美國將在12月下旬開始進行首次疫苗接種。

Moderna藥廠是在今年七月開始,大約3萬人分兩組開始疫苗試驗,其中1萬5千人使用疫苗,11人確診。另外一半1萬5千人,則使用沒有疫苗藥性的安慰劑(這種方式常用於藥物研究,以測試藥物的有效性),結果有185人確診。兩項試驗結合起來,相當於Moderna疫苗的有效性為94.1%。
另一項重要的數據是,接種疫苗確診的11人中沒有一個人是嚴重患者,但是使用安慰劑的185人中有30人是嚴重患者,其中一人死亡 。
Moderna疫苗對老年人和少數族裔人群也有相似的功效。
在輝瑞藥廠疫苗第三期臨床試驗中的有效性是95%,其中只有1名接種者是嚴重患者。
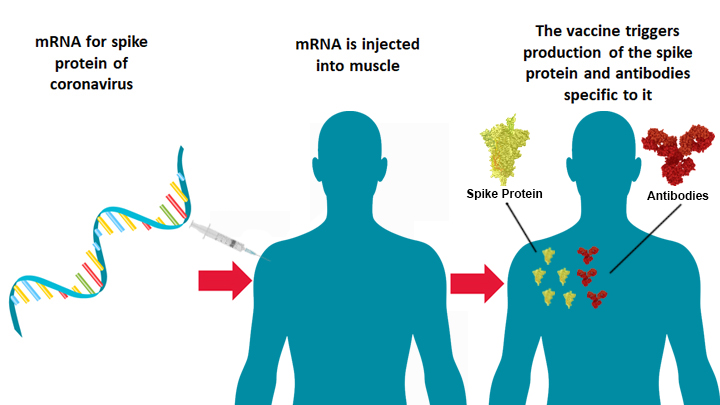
雖然輝瑞藥廠和Moderna藥廠的疫苗並不相同,但是這兩種疫苗都使用信使mRNA,使人體產生免疫反應。兩種疫苗都需分數週兩次注射,可能的副作用則有發燒或幾天的身體疼痛。
據了解,FDA疫苗審核會議的重點將在於,為何接種疫苗會染上新冠病毒,是不是因為接種者年紀或是本身就有的疾病,例如糖尿病有關。
FDA很有可能在審核會議後一兩天之內授權疫苗緊急使用,接著美國疾病控制與預防中心(CDC)就會對哪些族群應該先接受疫苗接種提出建議,第一批接受疫苗注射的很有可能是第一線醫護人員和療養院的居民。